Waarom wordt er bij sommige patiënten een bloedgas (astrup) afgenomen?
Je krijgt een indicatie van de oxygenatie (zuurstof opname) en de ventilatie (koolzuur afgifte), ook kun je het zuur-base evenwicht controleren.
Als eerste is het belangrijk om te vertellen dat je bij elke bloedgasanalyse de patiënt in je beoordeling mee moet nemen. Om te oefenen kan dit prima met alleen getallen, maar om daadwerkelijk iets te zeggen over de toestand van de patiënt moet je diens voorgeschiedenis en de actuele problemen ook meenemen. Zo is een verhoogd HCO3- bij een (voorheen) gezonde patiënt alarmerender dan een verhoogd HCO3- bij een chronisch dialyse patiënt.
Waarom is het zuur- base evenwicht belangrijk?
De zuurgraad van het bloed is: de mate waarin het bloed H+ ionen (waterstof ionen) bevat, weergegeven in PH.
De Ph is erg belangrijk voor een normale cel functie, wanneer deze niet binnen de normaal waarden is, zijn de cel functies niet optimaal.
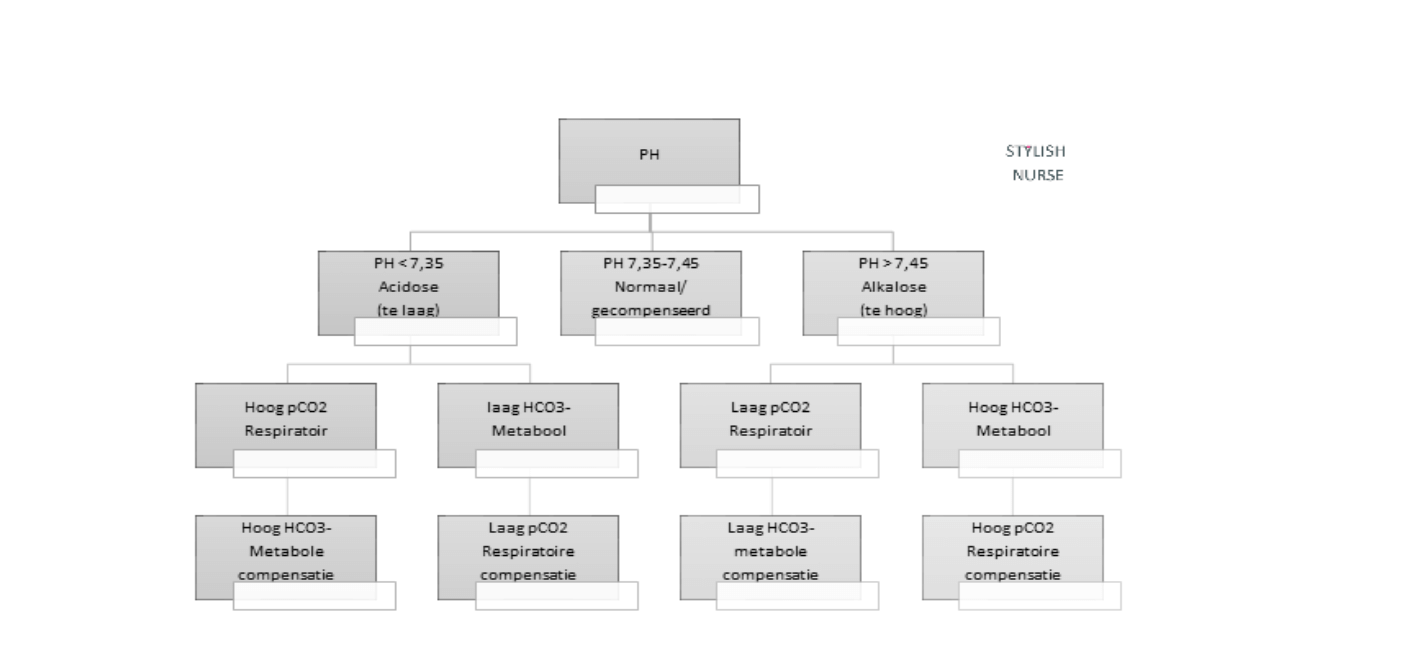
Acidose = zuur = veel H+ ionen = ph laag. Alkalose = basisch = weinig H+ ionen = ph hoog.
Hoe meer H+ ionen, hoe zuurder (dus lagere Ph).
Respiratoir = wanneer een zuur -base stoornis primair optreedt door een abnormale verandering van het pCO2.
Metabool = elke zuur- base stoornis die niet primair een respiratoire oorzaak heeft.
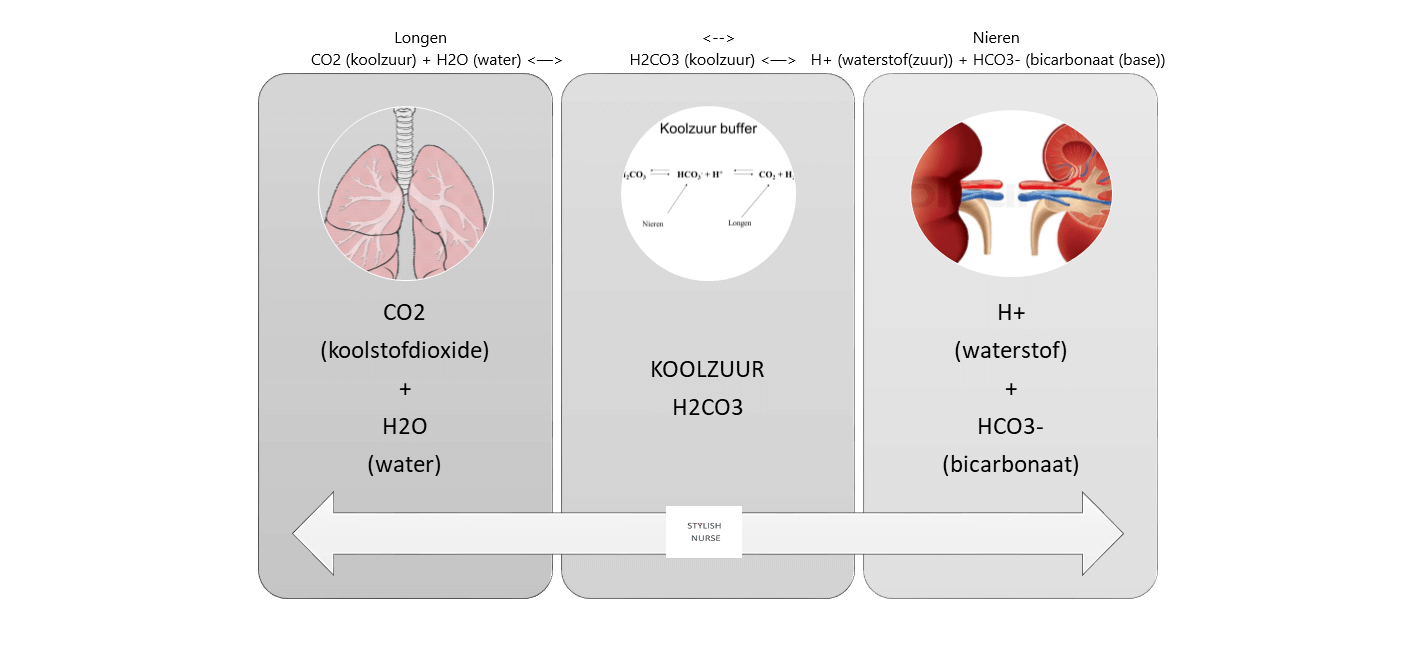
Regulatie mechanismen;
Koolzuur (=H2CO3-) is het product van verbranding met zuurstof in de cellen. Koolzuur (H2CO3-) gedraagt zich zowel als een voorraad van basen en zuren. Het staat bicarbonaat (HCO3-) af bij lage ph, om de zuren te binden waardoor de ph neutraliseert.
Koolzuur kan zich ook als zuur gedragen en staat dan waterstof ionen (H+) af om basen te binden waardoor de ph weer neutraliseert.
Het lichaam kan dit alles tijdelijk compenseren, zodat de cellen optimaal kunnen blijven functioneren. Aan dit compensatie mechanisme zit natuurlijk wel een limiet –> de patiënt kan daardoor in de problemen komen, de ph wordt dan te hoog of te laag en hierdoor zullen organen minder goed gaan functioneren.
Onder de afbeelding de 3 regelmechanismen in volgorde van snelheid.
Als eerste de intra- en extracellulaire buffers, dit is een compensatiemechanisme die binnen enkele seconden in werking treedt.
Als tweede de respiratiore regulatie, dit gaat binnen enkele minuten en tot slot de metabole regulatie, dit kost uren/ dagen.
1. Intra- en extracellulaire buffers;
Elke substantie die reversibel H+ ionen kan binden of afgeven.
- Intracellulair is dit Hb (base) of fosfaat (zuur).
- Extracellulair is dit bicarbonaat (HCO3-).
2. Respiratoire regulatie = snelle compensatie (minuten).
Je vergroot het ademminuut volume om zo meer koolzuur uit het bloed af te geven aan de longen en uit te ademen, dit kan binnen enkele minuten.
Voorbeelden:
Respiratoire acidose:
Door hypoventilatie (te laag AMV) is je pCO2 in het bloed verhoogd (= hypercapnie) en je Ph daardoor laag. Dit kan acuut zijn of chronisch. Wanneer dit acuut gebeurd: heb je een lage Ph, verhoogd pCO2 en HCO3- onveranderd.
Is dit chronisch (bijv. COPD) dan heb je normale Ph, verhoogd pCO2 en verhoogd HCO3- (zie 1e schema).
Respiratoire alkalose;
Hyperventilatie = te groot AMV. = hypocapnie. Je hebt dan een laag pCO2 en hoge Ph.
3. Metabole regulatie = langzame compensatie (dagen).
Je nieren kunnen extra H+ ionen uitscheiden of juist HCO3- resorberen met de urine.Wanneer iemand dan een verhoogd of verlaagd bicarbonaat heeft, weet je dat dit al enige tijd aan de gang is.
Voorbeelden:
Metabole acidose;
(Hierbij wordt ook nog onderscheid gemaakt tussen een normale- en een verhoogde anion gap, maar dat laat ik hier achterwege). Dit kan zijn door een verlaagd HCO3- door bijvoorbeeld diarree (verlies van HCO3-); nierfalen (onvermogen om H+ uit te scheiden en HCO3- te resorberen); intoxicaties met bijvoorbeeld spiritus of medicatie/ drugs; metformine intoxicatie of verhoogd lactaat; diabetische keto- acidose.
Metabole alkalose;
Toename van basen in het lichaam. Door bijvoorbeeld: infuus met HCO3-, bloedtransfusie (daarin zit citraat) afbraak ketenen waarbij HCO3- wordt gevormd, verlies H+ ionen via de nieren (bij diuretica), verlies H+ ionen bij braken / maagsonde of bij acute correctie van hypercapnie.